Сертификация FDA
Сертификация FDA является официальным подтверждением того, что продукция соответствует установленным Управлением по контролю за продуктами и лекарствами США (U.S. Food and Drug Administration) требованиям по безопасности, эффективности и качеству. Получение сертификата FDA свидетельствует о соответствии продукции нормам, применяемым к фармацевтическим препаратам, медицинским изделиям, пищевым продуктам, косметическим средствам и другим товарам, оказывающим влияние на здоровье и безопасность потребителей.
Значение сертификации FDA не ограничивается территорией Соединенных Штатов, поскольку она является международным стандартом качества и безопасности. Сертификация FDA выполняет важную коммерческую функцию. Наличие документа повышает доверие к компании со стороны профессионалов отрасли и конечных потребителей, а также усиливает конкурентные преимущества на глобальном рынке.
В данном материале речь пойдет о том, как пройти сертификацию FDA, какие документы запрашивает регулятор и какие преимущества в конечном итоге получит заявитель.
Что такое сертификация FDA
FDA сертификация (а точнее USFDA) — это международно-признанный стандарт, основная цель которого заключается в обеспечении высокого уровня качества и безопасности продукции, влияющей на здоровье человека. Данный стандарт применяется к пищевым продуктам, пищевым добавкам, косметике, лекарственным средствам, вакцинам, ветеринарным препаратам, медицинским устройствам и табачной продукции, производимой как на территории США, так и в других странах.
В соответствии с требованиями FDA, продукция может быть допущена к обороту на рынке только после прохождения обязательных испытаний, подтверждающих ее безопасность и соответствие установленным стандартам. В соответствии с законодательством США не существует единого государственного сертификата, подтверждающего качество товара. Вместо этого действует обязательная регистрация производителей и внесение конкретных продуктов в электронные реестры FDA. FDA сертификация и выполнение требований определяется активным статусом компании или продукта в официальных базах данных, что подтверждает их соответствие установленным стандартам безопасности и качества.
Федеральное управление по контролю за продуктами и лекарствами США не ограничивается выдачей сертификатов. Управление осуществляет постоянный мониторинг, клинические исследования и контроль качества продукции. При выявлении несоответствий требованиям FDA, Управление вправе приостановить действие сертификата или полностью его отозвать.
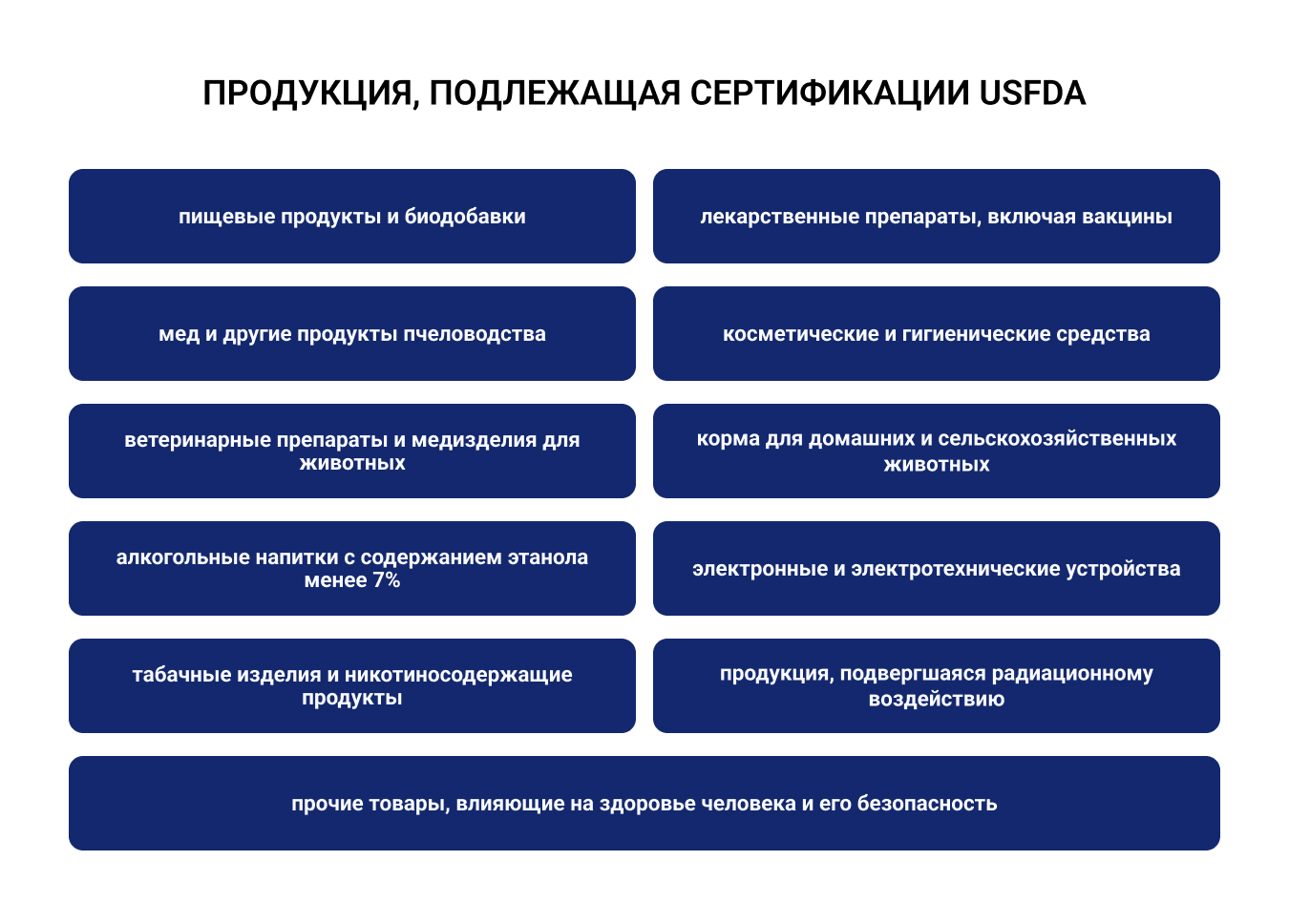
Продукция, подлежащая сертификации USFDA:
- пищевые продукты и биодобавки;
- лекарственные препараты, включая вакцины;
- мед и другие продукты пчеловодства;
- косметические и гигиенические средства;
- ветеринарные препараты и медизделия для животных;
- корма для домашних и сельскохозяйственных животных;
- алкогольные напитки с содержанием этанола менее 7%;
- электронные и электротехнические устройства;
- табачные изделия и никотиносодержащие продукты;
- продукция, подвергшаяся радиационному воздействию;
- прочие товары, влияющие на здоровье человека и его безопасность.
Независимо от того, производится ли продукция на территории США или только хранится и/или фасуется на складах, все складские помещения, участвующие в обороте продукции, подлежат обязательной регистрации в FDA с целью обеспечения отслеживания цепочки поставок. Сертификация FDA должна обновляться каждые два года.
FDA-approved и FDA-regulated — в чем разница
Прохождение сертификации FDA закреплено в Законе о пищевых продуктах, лекарствах и косметических средствах (Federal Food, Drug and Cosmetic Act), который обязывает производителей соблюдать установленные стандарты и проходить соответствующие процедуры контроля. Для юридических лиц это означает, что выход на рынок США требует либо прохождения процедуры регистрации и сертификации FDA, либо соблюдения установленных правил регулирования в зависимости от категории продукта.
FDA-approved
Термин FDA-approved в США означает, что конкретный продукт, будь то лекарство, медицинское устройство или иной регулируемый товар, прошел формальный процесс проверки и был одобрен FDA для конкретного применения. В юридическом смысле речь идет об официальном разрешении, предоставленном уполномоченным органом после оценки безопасности, эффективности и соответствия установленным стандартам. Для производителей и импортеров наличие статуса FDA-approved открывает законный доступ к продаже продукта на территории США, при этом любое отклонение от заявленных характеристик, состава или условий применения без повторного одобрения может повлечь юридическую ответственность, включая отзыв продукции, штрафы и даже уголовное преследование за нарушение федерального законодательства. FDA-approved касается конкретного продукта или марки, а не всей компании: одобрение не распространяется на производственные мощности, логистику или смежные товары, если они не прошли отдельную оценку.
FDA-regulated
В отличие от FDA-approved, статус FDA-regulated в США указывает на то, что продукт или деятельность компании подпадает под регулирование FDA, но не обязательно имеет официальное одобрение. Юридически это означает, что продукт подчиняется правилам контроля и стандартизации FDA, включая требования к маркировке, безопасности, клиническим испытаниям (для медицинских устройств и лекарств) и производственным процессам, однако фактическая проверка и выдача разрешения могут быть еще не завершены.
Например, многие пищевые добавки, косметика и устройства низкой и средней степени риска классифицируются как FDA-regulated: компания обязана соблюдать стандарты FDA, но формальное одобрение не требуется до выхода на рынок. С точки зрения закона этот статус все равно накладывает обязательства. То есть несоблюдение требований FDA-regulated может повлечь предупреждения, запреты на продажу, штрафы и обязательный отзыв продукции.
Почему получение сертификата FDA важно
Процесс сертификации продукции в США (FDA) для иностранных компаний связано с обеспечением ее соответствия установленным стандартам безопасности и качества. В первую очередь, любое предприятие, планирующее экспорт своей продукции в США, обязано пройти регистрацию объекта производства в реестре FDA Unified Registration and Listing System (FURLS), что предполагает официальное внесение данных о производственном объекте и назначение U.S. Agent — уполномоченного представителя на территории Соединенных Штатов, обеспечивающего прием официальной корреспонденции и уведомлений от регулятора. Одновременно с этим проводится листинг продукции, в ходе которого необходимо задокументировать все наименования ввозимых товаров, подлежащих сертификации, а также гарантировать соответствие упаковки и маркировки продукции стандартам, установленным в 21 CFR, включая наличие уникального 9-значного идентификатора юридического лица (DUNS).
Для иностранных участников рынка сложность представляет требование сертификации FDA в США, касающееся наличия физического представительства на территории страны. Федеральное законодательство предусматривает право FDA инициировать инспекции производства в любой точке мира, и в случае несоответствия предоставленных данных фактическим технологическим процессам, регистрация может быть аннулирована, что автоматически лишает компанию права экспорта в США.
Сертификация FDA выполняет ключевую функцию не только как юридический допуск к международному рынку, но и как гарант качества, подтверждая, что продукция безопасна для конечного потребителя, прошла соответствующие научные исследования и испытания, повышает доверие клиентов и партнеров, открывает возможности для выхода на премиальные сегменты рынка США, Канады, Европы и способствует конкурентному позиционированию компании на глобальной арене.
Процесс сертификации FDA: федеральные и отраслевые нормы
регулирование FDA в США закреплено в Food, Drug, and Cosmetic Act (FD&C Act), принятом в 1938 году. Этот закон наделил FDA широкими полномочиями по контролю за безопасностью и качеством пищевых продуктов, лекарственных средств и косметических товаров. Акт многократно пересматривался и дополнялся, отражая развитие биотехнологий, глобализацию торговли и новые подходы к защите здоровья потребителей. Любая попытка импорта продукции без соблюдения положений FD&C Act квалифицируется как федеральное правонарушение и влечет административную или уголовную ответственность.
Современная практика сертификации FDA в США существенно расширилась после введения в действие Food Safety Modernization Act (FSMA). Этот нормативный акт сместил акцент с реагирования на инциденты к их предотвращению: производители и импортеры обязаны документировать каждый этап производственного и логистического цикла. Ведение прозрачной цепочки поставок, контроль качества сырья и готовой продукции, а также оперативное уведомление о выявленных рисках стали обязательными требованиями.
Техническая регламентация процедуры сертификации FDA в США детализирована в Code of Federal Regulations (CFR). В CFR установлены стандарты идентичности продуктов, допустимые уровни пищевых добавок и лекарственных ингредиентов, а также требования к маркировке и упаковке. В последние годы особое внимание уделяется реформе MoCRA (Modernization of Cosmetics Regulation Act), которая привела к усиленному контролю за косметической отраслью, включая обязательный сбор и отчетность о серьезных побочных эффектах даже для бытовых средств гигиены.
Другие нормативные акты, в соответствии с которыми проводится сертификация продукции по требованиям FDA:
- Medical Device User Fee and Modernization Act — регулирует сборы за регистрацию медицинских изделий и ускоряет процессы рассмотрения заявок.
- Food and Drug Administration Safety and Innovation Act — укрепляет полномочия FDA в области инновационных медицинских и биотехнологических продуктов.
- Public Health Security and Bioterrorism Preparedness and Response Act — устанавливает требования к защите цепочки поставок и предотвращению умышленного загрязнения продуктов.
- Good Manufacturing Practice — устанавливает стандарты для всех этапов производства, хранения и дистрибуции продукции.
Федеральный FD&C Act дополняется отраслевыми руководствами (Guidance Documents), которые являются обязательными для прохождения инспекций и аудитов. Соблюдение стандартов регулирования сертификации FDA в США является обязательным условием для законного обращения продукции на территории страны, и любое отклонение от установленных норм рассматривается как угроза общественному здоровью и безопасности потребителей.
Как получить сертификат FDA
Чтобы успешно пройти процесс сертификации FDA, необходимо оценить соответствие продукции федеральным требованиям, провести аудит производственной площадки и убедиться в безопасности всех ингредиентов. Ключевым аспектом является определение категории товара, так как от этого напрямую зависят объем необходимых испытаний, государственные сборы и сроки рассмотрения заявки. Для иностранных компаний сертификация FDA связана с обеспечением прозрачности всей цепочки поставок, что позволит исключить юридические и таможенные риски.
Процесс оценки готовности продукции к сертификации FDA в США включает детальный анализ состава товара, материалов упаковки и соблюдение всех нормативных требований США. Вся документация должна быть подготовлена на английском языке и оформлена в соответствии с отраслевыми руководствами FDA.
Основные этапы регистрации и сертификации FDA в США:
- Идентификация и классификация продукта.
- Получение идентификатора DUNS и назначение агента.
- Подготовка технического файла и листинг.
- Оплата сборов и получение сертификата FDA в США.
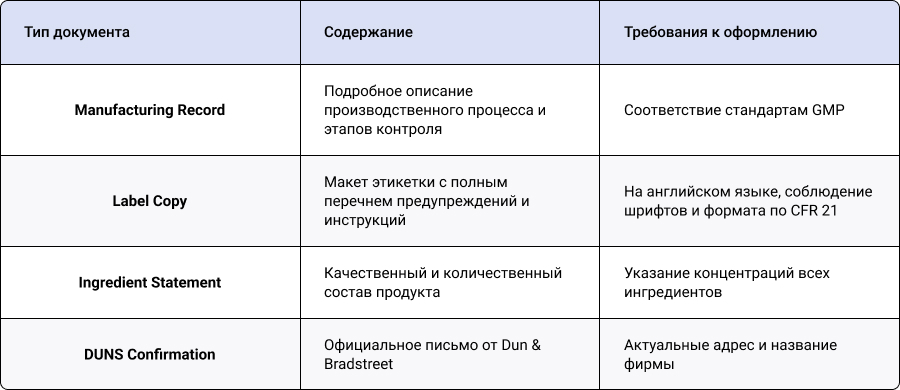
На первом этапе производитель определяет юридический статус товара (пищевой продукт, косметика, медицинское изделие или биологически активная добавка). Продукт сопоставляется с соответствующими разделами федерального кодекса CFR 21. Это позволяет определить размер государственных сборов, определить необходимость клинических исследований и установить перечень документов для подачи. Для работы с федеральными порталами требуется регистрация в системе Dun & Bradstreet и получение девятизначного кода DUNS. Одновременно с этим заключается договор с резидентом США, который будет официально представлять компанию перед FDA и принимать юридическую корреспонденцию. На следующем этапе должен быть подготовлен полный комплект документов. В таблице указан контрольный список документов для подачи:
Данные подаются через электронные системы FURLS или CDER Direct, включая информацию о предприятии и каждой товарной позиции, предназначенной для экспорта. После проверки всех данных заявитель оплачивает установленные государственные сборы, ему присваивается регистрационный номер, который подтверждает, что компания исполнила обязательства по уведомлению. В среднем оформление сертификата FDA в США занимает от 2 недель для пищевых товаров и от 6 месяцев для медицинских изделий.
Регулирование продукции FDA в США: сферы ответственности
Федеральное управление по контролю за продуктами и лекарствами США отвечает не только за пищевую продукцию и лекарственные средства, но и за устройства, косметику, добавки и оборудование, способное оказывать биологическое, химическое или радиационное воздействие на человека.
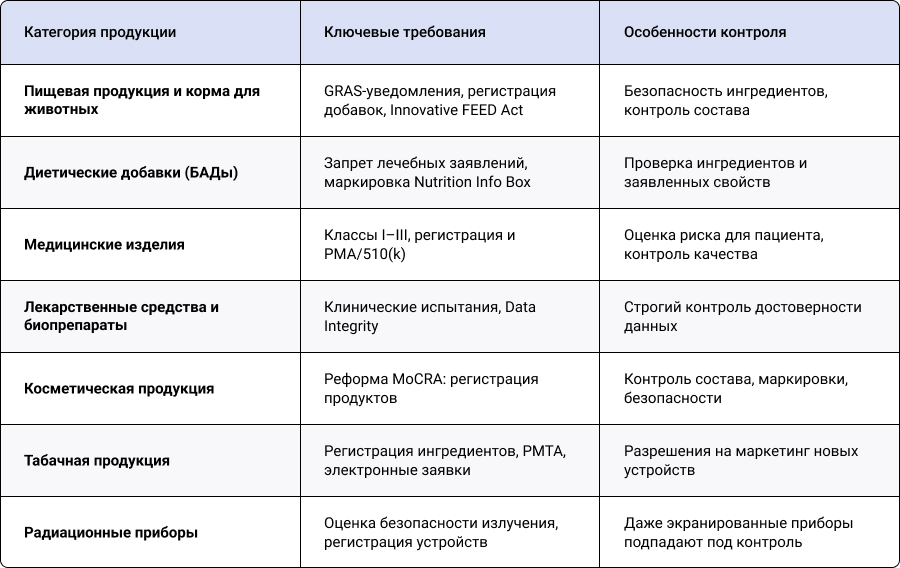
Контроль FDA в США распространяется как на продукцию, произведенную в стране, так и на импортируемые товары, при этом каждая категория регулируется отдельными нормативными актами (закрепленными в CFR 21), предусматривающими детальные требования к составу, маркировке, безопасности и испытаниям.
Пищевая продукция и корма для животных
FDA осуществляет контроль за безопасностью пищевых продуктов, включая напитки, фрукты, овощи, мясо, морепродукты и готовые к употреблению блюда. С 2026 года вступает в силу требование уведомления о компонентах с признанным статусом GRAS (Generally Recognized as Safe), исключающее возможность одностороннего признания ингредиента безопасным без информирования регулятора. В эту категорию также входят корма для животных. Innovative FEED Act позволяет рассматривать некоторые зоотехнические добавки, например, снижающие выбросы метана, как пищевые ингредиенты, а не как лекарства, что упрощает их регистрацию и использование.
Диетические добавки (БАДы)
Диетические добавки регулируются FDA отдельно от лекарственных средств. Продажа БАДов не требует предварительного одобрения, однако запрещено размещать лечебные заявления на упаковке. Основное внимание уделяется проверке состава, безопасности ингредиентов и корректности заявленных свойств. С 2025 года введена обязательная фронтальная маркировка Nutrition Info Box, информирующая потребителя о содержании сахара, натрия и других потенциально вредных компонентов.
Медицинские изделия и техника
Сертификация медицинских изделий согласно требованиям FDA в США распространется на три класса в зависимости от потенциального риска для пациента:
- Класс I (низкий риск) — изделия, требующие базовой регистрации, например, бинты, маски.
- Класс II (средний риск) — изделия, подлежащие уведомлению 510(k), включая аппараты УЗИ и шприцы.
- Класс III (высокий риск) — изделия с критическим воздействием на жизнь пациента, например, кардиостимуляторы, требующие предварительного научного одобрения (PMA).
Каждый класс имеет отдельные требования к тестированию, контролю качества и документообороту, обеспечивая системное управление рисками.
Лекарственные средства и биопрепараты
Сертификация FDA лекарств в США распространяется на каждый новый препарат и связана с обширными клиническими исследованиями. С 2026 года акцент сделан на проверке целостности данных (Data Integrity), исключающей подачу недостоверных или фальсифицированных результатов испытаний в заявках на получение сертификата FDA на лекарственное средство.
Косметическая продукция
С середины 2024 года (как часть реформы MoCRA) регистрация косметических продуктов стали обязательными для всех производителей, кроме микропредприятий. Управление теперь отслеживает состав, безопасность и маркировку косметики, что делает соблюдение требований сертификации FDA необходимым условием для законного оборота продукции на рынке США.
Радиационные приборы и табачная продукция
FDA осуществляет надзор за табачной продукцией, включая электронные устройства, требуя обязательной регистрации ингредиентов и разрешений на маркетинг новых продуктов через портал CTP. С января 2026 года все заявки PMTA подаются исключительно в электронном формате. Радиационные приборы, включая рентгеновские установки, лазеры, микроволновые печи и другие устройства, генерирующие излучение, подпадают под обязательный контроль FDA даже при полном экранировании, поскольку любое потенциальное воздействие на здоровье человека требует оценки безопасности.
Экспортные сертификаты FDA
При международных поставках продукции из США ключевым инструментом подтверждения ее законного производства и обращения является экспортный сертификат, выдаваемый U.S. Food and Drug Administration. Этот документ используется иностранными регуляторами и таможенными органами для подтверждения возможности ввоза продукции, произведенной в США. Сертификат FDA удостоверяет статус товара и содержит официальные сведения о производителе на основании данных федеральных реестров.
Запрос на получение экспортного сертификата FDA подается через электронную систему CECATS (Centralized Export Certification Application Tracking System). Процесс рассмотрения включает проверку регистрации производителя, листинга продукции и соответствия категории товара требованиям действующих регуляторных норм. Существуют несколько форм сертификатов FDA, применяемых в зависимости от категории продукции и целей внешнеторговой операции:
- Certificate to Foreign Government (CFG) — для медицинских изделий и лекарственных препаратов, который подтверждает соответствие продукции федеральным требованиям и дает право импортировать ее в страну назначения.
- Certificate of Free Sale (CFS) — удостоверяет законное обращение товара на рынке США и используется для подтверждения внутренней легальности продукции при экспорте.
- Certificate of Exportability (COE) — оформляется на продукцию, разрешенную к экспорту при наличии ограничений на внутреннее обращение.
Специализированные сертификаты выдаются для кормов, ветеринарной продукции, пищевых и косметических товаров по требованию иностранных регуляторов с учетом специфики отрасли. Распространена практика оформления электронных сертификатов FDA для экспорта, что ускоряет верификацию и упрощает взаимодействие с иностранными регуляторами.
Заключение
Сертификация FDA в США является обязательным условием для законной торговли определенными категориями товаров на территории страны. Это обязательный этап подготовки к выходу на американский рынок как в онлайн-продажах (например, на платформах вроде Amazon), так и в традиционной офлайн-торговле. Наличие регистрации FDA в США документально фиксирует соответствие продукции установленным стандартам качества и безопасности, обеспечивая защиту прав и интересов конечного потребителя.
Для предпринимателей, планирующих вести бизнес в США, регистрация в FDA может показаться сложной и индивидуально ориентированной процедурой. Ошибки или упущения могут привести к задержкам или отказу в регистрации, что ограничивает возможность законной продажи товаров на рынке. Своевременное привлечение профильных экспертов позволяет оптимизировать процесс регистрации, минимизировать риски и гарантировать соответствие всем нормативным требованиям FDA. Сопровождение сертификации FDA для иностранных компаний позволяет ускорить выход продукции на рынок и обеспечить юридическую защищенность бизнеса на территории США.
Источник: https://ybcase.com